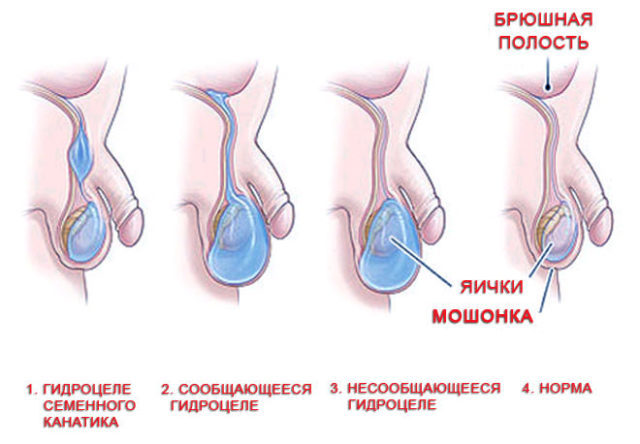
Hvorfor er prostata intraepitelial neoplasi farlig?
Intraepiteliale neoplasier

Offisiell statistikk registrerer årlig 10 millioner tilfeller av kreft i verden, og 30% av ondartede svulster er virusavhengige, dvs. neoplasmer har økt eller høy risiko for å utvikle seg i nærvær av virusinfeksjoner i kroppen.
I strukturen for onkologisk sykelighet i befolkningen i St. Petersburg utgjør virusavhengige svulster omtrent 40% hos menn og mer enn 30% hos kvinner. De siste årene har forholdet mellom HPV og dysplasi og plateepitelkarsinom i livmorhalsen blitt vist (Gaidukov S. N. og så videre.
, 2004), samt kreft i hode og nakke (Safronnikova N. R., Merabishvili V. M., 2005).
I tillegg til de klinisk avgrensede manifestasjonene av PVI, skilles også subkliniske og latente former for infeksjon, så vel som HPV-assosierte sykdommer (Handlley Y. et al., 1994). De betraktes iboende som intraepiteliale neoplasier av varierende alvorlighetsgrad. Dermed sa Bosch F. et al.
(2002) viste at mer enn halvparten av kvinnene med anogenitale papillomer har cervikale intraepiteliale neoplasier (CVI I - III). I utenlandsk litteratur er navnet cervical intraepithelial neoplasia (CIN) av varierende alvorlighetsgrad mye brukt.
Alle disse patologi -variantene kombineres under navnet intraepiteliale neoplasier (VN) eller plateepitelige intraepitelielle lesjoner (SIL). Det skal bemerkes at CVN I (CINI) er synonymt med begrepet "svak dysplasi", som er mer kjent for den russiske leseren.
CVI II (CIN II) tilsvarer "moderat dysplasi". CVI III (CIN III) brukes for å referere til både "alvorlig dysplasi" og preinvasivt karsinom (tabell 2). 5, 6).
I tillegg til begrepene cervikal intraepitelial neoplasi (CIN), inneholder utenlandsk litteratur og begrepene "vulvar intraepitelial neoplasia (VIN)", "penile intraepithelial neoplasia (PIN)" (Ludicke F. et al, 2001).
Inverterte (eller endofytiske) vorter er på mange måter identiske med flate vorter, Imidlertid har de evnen til pseudo-invasivt å trenge inn i underliggende stroma eller åpninger kjertler. Endofytiske vorter har mange morfologiske trekk, som ligner karsinom in situ, som de kan være assosiert med.
Den cytologiske markøren for HPV -infeksjon er påvisning av coilocytter. Coilocytter er celler i plateepitel på overflaten eller mellomliggende lag, som har en uttalt opplysningssone rundt kjernen, den såkalte "perinuclear halo". Dens opprinnelse er forbundet med delvis nekrose av cytoplasma i perinukleære sonen som et resultat av cytopatisk virkning.
I periferien av de nekrotiske områdene konsentreres cytoplasmatiske fibriller, noe som fører til en skarp begrensning av perinukleære soner. De første manifestasjonene av HPV -lesjoner er preget av tilstedeværelsen av enkle vakuoler i perinukleære sonen. Begrepet "koilocytisk dysplasi" ble introdusert av StegnerH.S. (1981).
Noen forfattere merker tilstedeværelsen av såkalte "stemplede vakuoler" i coilocytter, "cytoplasma ballong". HPV -infeksjon er preget av påvisning av epitelceller med varierende grad av keratinisering og binukleatede og flerkjernede celler.
I tillegg til koilocytisk atypi er manifestasjonen av HPV-infeksjon akantose, spredning av basalceller, metaplasi, hyper-, para-, dyskeratose av overflatelagene i epitelet, tilstedeværelsen av mitose.
Alt dette mangfoldet kompliserer den kliniske klassifiseringen av denne patologien. I 1994 g. J. Handley og W. Dismure, basert på egen erfaring og analyse av litteraturdata, foreslo en klassifisering av kliniske former for HPV -infeksjoner og relaterte sykdommer (Handlley Y.
et al., 1994). Det er til en viss grad konvensjonelt og skjematisk, men generelt gjør det det mulig å presentere et komplett bilde av de kliniske manifestasjonene av denne patologien. Bord 5 viser klassifiseringen av former for anogenital PVI.
Den viser de forskjellige kliniske formene som er synlige for det blotte øye eller usynlige. Subkliniske former er asymptomatiske, detekteres bare ved kolposkopi eller cytologiske, histologiske studier.
Latente former er preget av fravær av endringer registrert på cytologisk og histologisk nivå.
Tabell 5. Former for manifestasjon av anogenital HPV -infeksjon (Handlley J., Dinsmore W., 1994)
| Funksjoner i flyten | Manifestasjonsformer |
| Kliniske former | Vorter (kjønnsvorter, flatvorter, vulgære vorter) |
| Symptomatisk VL (CIN, VIN, PIN) i de tidlige stadiene - coylocytose, dyskeratose, i fravær av dysplasi (flatvorter) | |
| Subkliniske former | Asymptomatisk VL (CIN, VIN, PIN) i de tidlige stadiene av coylocytose, dyskeratose i fravær av dysplasi |
| Latente former | Fravær av morfologiske eller histologiske endringer. Påvisning av humant papillomavirus -DNA |
Det er visse vanskeligheter med å identifisere den klassiske HPV -infeksjonen som oppstår i form av godartede lesjoner (flate vorter, subkliniske former for sykdommen).
Som regel, med lesjoner bare assosiert med HPV, merkes uttalt akantose med mindre karakteristisk dyskaryose enn med dysplasi med samtidig infeksjon, når alvorlighetsgraden av koilocytisk atypi med en økning i dysplastiske prosesser reduseres.
Ved malignitet vises følgende symptomer: pleomorfisme, anaplasi av cellulære elementer, utseendet umodne epitelceller med klassiske tegn på malignitet (basofili, forstørrelse av kjernen, innholdet i atypisk kromatin).
Fant spesifikke morfologiske endringer i bowenoid papullose: i dette tilfellet er det notert hyperparakeratose, granulose, vakuolisering av keratinocytter i kombinasjon med akantose, inflammatoriske infiltrater i dermis. I epidermis er det tegn på atypi, patologiske mitoser og keratinocytter med hyperkromiske kjerner. Pigmentet melanin finnes i epitelcellene og melanofager i papillene i dermis.
Det er visse vanskeligheter med å identifisere den klassiske HPV -infeksjonen som oppstår i form av godartede lesjoner (flate vorter, subkliniske former for sykdommen).
Som regel, med lesjoner bare assosiert med HPV, merkes uttalt akantose med mindre karakteristisk dyskaryose enn med dysplasi med samtidig infeksjon, når alvorlighetsgraden av koilocytisk atypi med en økning i dysplastiske prosesser reduseres.
Ved malignitet vises følgende symptomer: pleomorfisme, anaplasi av cellulære elementer, utseendet umodne epitelceller med klassiske tegn på malignitet (basofili, forstørrelse av kjernen, innholdet i atypisk kromatin).
Fant spesifikke morfologiske endringer i bowenoid papullose: i dette tilfellet er det notert hyperparakeratose, granulose, vakuolisering av keratinocytter i kombinasjon med akantose, inflammatoriske infiltrater i dermis. I epidermis er det tegn på atypi, patologiske mitoser og keratinocytter med hyperkromiske kjerner. Pigmentet melanin finnes i epitelcellene og melanofager i papillene i dermis.
Rollen til kombinert papillomavirus og herpetiske infeksjoner i malignitet i livmorhalsens epitel. Det er vist at omtrent 15% av de klinisk friske kvinnene er smittet med HPV, og derfor er de utsatt for risiko.
Serologisk undersøkelse av kvinner med stadium 2-3 livmorhalskreft (CC) avslørte en uttalt sammenheng mellom klinisk diagnose og tilstedeværelse av antistoffer mot HPV og HSV-1, men det ble imidlertid ikke funnet noen sammenheng mellom tumorutvikling og vogn HSV-1.
Dette bekrefter oppfatningen om at transport av HPV ikke er en tilstrekkelig betingelse for malignitet. En viktig rolle i utviklingen av tumorprosesser, som en samtidig faktor, tildeles herpesvirus.
Når man studerte innflytelsen av HSV-1-genomet på HPV-18-replikasjon, ble HeHa- og A431-cellelinjer som bærer genomet til HPV-18-viruset infisert med HSV-1-viruset. Deretter ble den aktive stimuleringen av reproduksjonen av HPV-18-viruset bestemt.
Videre stimulerte HSV-1 ikke bare HPV-replikasjon, men bidro også til integrering av genomet i genomet til vertscellen, som er en viktig betingelse for tumortransformasjon (Naga Y. et al., 1997).
Det bør bemerkes den mulige rollen til HSV-2 (i forbindelse med papillomavirus, CMV, klamydia og mykoplasma) i utviklingen av neoplastiske prosesser hos mennesker, spesielt livmorhalskreft og prostatakreft. Det antas at i dette tilfellet kan HSV-2 fungere som en kofaktor for karsinogenese, starte utviklingen av dysplasi og opprettholde den i en tilstand av stabilisering. Det ble konkludert med at nøkkelrollen for induksjon av tumorprosessen spilles av HPV-16, HPV-18 og HSV-2 i kombinasjon med ytterligere faktorer, hvis art fortsatt er uklart og krever avklaring (Dmitriev G. A., Bitkina O. A., 2006; Kiselev V. OG. et al., 2000).
Tabell 6. HPV-assosierte sykdommer (Handlley J., Dinsmore W., 1994)
| Former av sykdommen | Sykdomens stadium | Manifestasjonsformer |
| Subklinisk | Tidlig BHI | Mild dysplasi, kan være koylocytose, dyskeratose |
| Sent BHII | Alvorlig dysplasi, kan være koylocytose, dyskeratose | |
| VHIII | Alvorlig dysplasi eller karsinom in situ, kan være coylocytose, dyskeratose | |
| Klinisk | — | Mikroinvasivt plateepitelkarsinom |
BRUK AV CYCLOFERON I TERAPI AV PAPILLOMAVIRUS INFEKSJON
Anbefalinger til leger
Kilde: https://medi.ru/info/7716/
Analyse av resultatene av biopsier og rebiopsier av prostata i urologisk distriktsavdeling i det vestlige administrative distriktet St. Moskva over en treårsperiode

I dag er prostatakreft (PCa) et av de viktigste medisinske problemene. Dette skyldes det faktum at prostatakreft er den vanligste solide svulsten i Europa (ifølge data for 2004.
, den estimerte forekomsten var 214 000 tilfeller) og overstiger forekomsten av lungekreft og tykktarmskreft [1]. I tillegg er PCa for tiden den nest største dødsårsaken av ondartede neoplasmer hos menn [2]. I Russland vokser forekomsten av prostatakreft jevnt og trutt: for perioden 1999-2009.
den økte fra 15,69 til 38,41 per 100 þús. befolkning (+ 144,8%) og er 10,7% i strukturen av kreftforekomst hos den mannlige befolkningen [3].
Utbredt screening av menn for påvisning av prostatakreft ved å bestemme nivået av prostata-spesifikt antigen (PSA) har ført til en betydelig økning i antall transrektale biopsier i prostatakjertelen - metoden betraktet som "gullstandarden" i kreftdiagnose prostata. En biopsi av prostata, utført når det er indikert og utført ved bruk av den beste teknikken, gir legen det nødvendige informasjon om pasienten har en forstadier til kreft (prostata intraepitelial neoplasi av høy kvalitet) eller kreft prostata.
I tillegg, ifølge biopsi av prostata, kan legen bestemme lokalisering og omfang av svulsten i biopsiprøven, tilstedeværelsen perineural invasjon eller invasjon av prostatakapsel, stadium av differensiering av tumorceller (gradering på en skala Gleason).
Disse indikatorene, i kombinasjon med andre kliniske data, gjør det mulig å fastslå stadium (T) og graden av risiko. sykdomsprogresjon og / eller tilbakefall etter radikal prostatektomi eller annen terapeutisk behandling innblanding.
Les også:Årsakene til utseendet til mikropenis hos menn i forskjellige aldre
Uten denne informasjonen er det umulig å velge riktig behandlingsmetode og bestemme strategien for videre pasientbehandling, og derfor å tolke resultatene av en prostatabiopsi er en av de viktigste oppgavene en spesialist står overfor innen urologi og onkologi.
Materialet samles hovedsakelig langs de perifere delene av kjertelen, der tidlige former for prostatakreft hovedsakelig oppdages.
I en transrektal biopsi går nålen i skrå retning bakfra og foran [4], mens en stor mengden vev i hyperplastiske overgangssoner, volumet av vev tatt fra den perifere sonen under atrofien er signifikant mindre.
Til tross for at denne metoden regnes som "gullstandarden" for diagnostisering av prostatakreft, øker antallet gjentatte biopsier. Ifølge forskjellige forfattere er bare 17–33% av biopsiene positive [5].
Hva er årsaken til den lave sensitiviteten til diagnosen "gullstandard" av prostatakreft? I mange tilfeller, ved analyse av den patomorfologiske undersøkelsen av biopsiprøven, endres ikke-ondartede endringer i kjertelen epitel forbundet med økt risiko for å utvikle prostatakreft hos en pasient og krever derfor gjentagelse biopsi. Slike alarmerende funn inkluderer atypi med mistenkt adenokarsinom eller atypisk liten acinar -spredning (ASAP) og IDUer. Diagnosen IDU stilles når kjertler finnes i biopsiprøven, acini og kanaler som er foret med atypiske celler, men et intakt basallag er tilstede, som skiller PIN -koder fra adenokarsinomer. Det antas at IDU er en forstadier til kreft som kan ha høy eller lav grad av neoplasi, avhengig av spekteret og alvorlighetsgraden av de observerte neoplastiske endringene.
Tidligere studier har vist at høyverdige IDUer er forbundet med en risiko på 27–65% for å oppdage prostatakreft med rebiopsy [6], men nyere arbeid, inkludert data fra utvidede biopsier, antyder at risikoen fremdeles ikke er så høy og er omtrent 10–20%. Som anbefalt av National Comprehensive Cancer Network (NCCN), hvis en IDU av høy kvalitet blir funnet etter en standard sekstantbiopsi (eller biopsi med antall prøver tatt mindre enn 10), er det nødvendig etter 3 måneder å utføre en ny biopsi ved hjelp av en utvidet teknikk (10 eller flere biopsier). Hvis en forlenget biopsi ble utført fra begynnelsen, bør pasienten biopsieres på nytt 6–12 måneder senere ved hjelp av en utvidet eller metningsteknikk.
Begrepet "atypisk liten acinar -spredning" ble først foreslått av K. Iczkowski for å karakterisere kjertler med tegn på arkitektonisk og cellulær atypi som ikke kan tilskrives reaktiv atypi, atypisk adenomatøs hyperplasi, PIN eller prostatisk adenokarsinom.
ASAP er ikke en forstadier til kreft, men uttrykker bare tvetydigheten i diagnosen, det vil si at med ASAP kan man ikke å si med sikkerhet om det observerte bildet tilsvarer adenokarsinom eller godartet nederlag.
I denne forbindelse anbefales det å konsultere en annen spesialist (helst en ekspert når du mottar en ASAP -diagnose) nivå) med revisjon av histologiske briller, er det mulig å bruke immunhistokjemiske analysemetoder biopsier.
Det har blitt vist at atypi med mistenkt kreft er assosiert med en omtrent 50% sannsynlighet for adenokarsinomdiagnose hos gjentatt biopsi, og lokaliseringen av adenokarsinom tilsvarer i de fleste tilfeller stedet for det tidligere oppdagede atypia. I følge P.
Humphery, i 18–75% av tilfellene er fokuset på adenokarsinom skjult under ASAP [7].
Det er derfor, innen 3 måneder etter den første biopsien, anbefales det å utføre en ny biopsi ved hjelp av den forlengede ordningen, og for å øke diagnostiske verdien av rebiopsy, anbefaler NCCN å ta flere prøver fra stedet atypia.
Hvis det ikke blir funnet kreft ved gjentatt biopsi, må du observere nøye med periodisk måling av PSA -nivåer, digital rektalundersøkelse og gjentatt biopsi (det er imidlertid kjent at to gjentatte biopsier etter den første er nok til å diagnostisere de aller fleste svulster prostata).
Materialer og metoder
Vi gjennomførte en studie for å analysere resultatene av gjentatte prostatabiopsier utført for tilstedeværelse av høyverdige IDUer og ASAP i den primære biopsien. Studien inkluderte 932 menn over 50 år, som i 2009–2011.
ble sendt til distriktsurologiavdelingen på grunnlag av bypoliklinikken nr. 147 i det vestlige distriktet i Moskva for videre undersøkelse på grunn av mistenkt prostatakreft. Pasientene ble målt for PSA -nivåer og gjennomgikk fysisk undersøkelse, inkludert digital rektal og transrektal ultralyd av prostata.
Pasienter med PSA-verdier større enn 4 ng / ml gjennomgikk en 12-punkts transrektal multifokal prostatabiopsi etterfulgt av histologisk undersøkelse, inkludert bestemmelse av graden av aggressivitet av prostatakreft på en skala Gleason. Alderen til pasientene varierte fra 50 til 79 år, og gjennomsnittsalderen var 62 år.
Ifølge resultatene av histologisk undersøkelse ble prostatakreft påvist hos 40% av pasientene (n = 371). Gjennomsnittlig PSA -nivå blant alle pasientene var 14,6 ng / ml. Hos 65% (n = 607) av pasientene med diagnostisert prostatakreft var PSA-verdien i den såkalte "gråsonen" (4–10 ng / ml).
Gjennomsnittlig PSA-verdi for den "grå sonen" for denne gruppen pasienter var 6,7 (4,02-9,85) ng / ml. Det ble gjort en analyse av forholdet mellom PSA -nivået og Gleason -indeksen (tab. 1). Fordelingen av pasienter etter lav og høy grad av IDU og ASAP er presentert i tabell 2.
resultater
Ved evaluering av det histologiske materialet ble det avslørt at omtrent 23% (n = 214) av biopsier inneholdt høyverdige IDUer i kombinasjon med forskjellige bakgrunnspatologier (BPH, kronisk prostatitt). PCa ble bekreftet i 40% (n = 371) av tilfellene. Kombinasjonen av PIN + PCa ble funnet i 4,1% (n = 39) av histologiske prøver.
Hvis 13,3% (n = 124) av biopsiene i aldersgruppen 50–59 år inneholdt IDU, så var andelen i alderen 70–79 år 11,2% (n = 105).
Når gjentatte biopsier ble utført hos 16 pasienter med høyverdige IDUer etter 3 måneder, ble prostatakreft påvist i 6 (37,5%) tilfeller, etter 6 måneder hos 28 pasienter var antallet verifiserte PCa 13 (46,4%), etter 12 måneder hos 14 pasienter ble ytterligere 4 (28,5%) tilfeller oppdaget PCa.
ASAP ble påvist hos 89 pasienter (9,5%). 68 pasienter gjennomgikk gjentatte biopsier etter 3 måneder.
Resten av diagnosen prostatakreft ble bekreftet som et resultat av revisjon av det histologiske materialet ved bruk av immunhistokjemiske analysemetoder.
Blant de 68 pasientene med ASAP som gjennomgikk en ny biopsi etter 3 måneder, ble diagnosen prostatakreft diagnostisert i 26 tilfeller (38,2%). Blant pasienter med ASAP og høyverdige IDUer, av 11 gjentatte biopsier, ble prostatakreft påvist hos 10 pasienter (90,1%).
konklusjoner
Således ble diagnosen prostatakreft innen 1 år bekreftet hos 23 (39,6%) av 58 pasienter med høyverdige IDUer med gjentatt biopsi.
Deteksjonshastigheten for prostatakreft i nærvær av ASAP i vår studie var henholdsvis 38,2% og 90,1% i nærvær av ASAP og en kombinasjon av ASAP med høyverdige IDUer i biopsiprøven. Vår studie bekreftet at høy klasse IDU er en forstadier til kreft.
Resultatene av denne studien indikerer at identifisering av høyverdige IDUer og ASAP er en indikasjon på prostata rebiopsy.
Kilde: http://umedp.ru/articles/_analiz_rezultatov_biopsiy_i_rebiopsiy_predstatelnoy_zhelezy_v_okruzhnom_urologicheskom_otdelenii_za.html
Cervikal intraepitelial neoplasi - CIN (cervikal dysplasi)

19. juni 2018
Livmorhalsens viktigste patologi, som er livstruende for en kvinne, er livmorhalskreft (CC). En kvinne dør av livmorhalskreft annethvert minutt i verden. Globalt er livmorhalskreft nå den tredje ledende årsaken til kreftdød hos kvinner, etter bryst- og lungekreft.
Mer enn 12 500 nye tilfeller av livmorhalskreft registreres årlig i Russland, mer enn 6000 kvinner dør årlig.
Det siste tiåret har det vært en klar økning i forekomsten av livmorhalskreft blant unge kvinner i aldersgruppen under 40 år, og økningen i forekomsten i gruppen kvinner under 29 år er spesielt merkbar.
Kreftutviklingen går foran dysplasi av livmorhalsens epitel.
Moderne navn livmorhalsdysplasi - cervikal intraepitelial neoplasi (CIN). Dette er en patologisk prosess, ledsaget av utseende i tykkelsen på epitelaget av atypiske celler med forskjellige graden av svekkelse av differensieringen, som deretter påvirker alle lag av celler i det lagdelte plateepitelepitelet i nakken livmor.
Fører til
Hovedårsaken til utviklingen av CIN er infeksjon av en kvinne med onkogene typer. humant papillomavirus (HPV), som inkluderer: 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66, 68, 73, 82. Imidlertid fører ikke hver infeksjon til utvikling av CIN og dets progresjon til livmorhalskreft. Dette krever predisponerende faktorer:
- tidlig alder for første samleie (opptil 16 år);
- hyppig endring av seksuelle partnere;
- svekkelse av lokal immunbeskyttelse, manifestert av en signifikant nedgang i type A og G immunglobuliner i slimet i livmorhalskanalen;
- langvarig forløp av inflammatoriske prosesser i kjønnsorganene på grunn av bakteriell infeksjon, infeksjoner, seksuelt overførbar sykdom - klamydia, genital mykoplasmose, trichomoniasis, cytomegalovirus, herpes simplex -virus 2 typer;
- hyppige tilbakefall av bakteriell vaginose;
- avvik fra resultatene av cytologiske utstryk fra normen;
- HIV -infeksjon;
- hyppig fødsel, spesielt komplisert av traumer i fødselskanalen;
- to eller flere kirurgiske aborter;
- aktiv og passiv røyking øker risikoen for å utvikle CIN med 4 ganger;
- individuell genetisk disposisjon for gynekologiske ondartede neoplasmer - 1,6 ganger øker risikoen for å utvikle sykdommen;
- mangel på matprodukter av folat, betakaroten, vitamin A og C fører til forstyrrelse av hormonmetabolismen i leveren;
- kvinner med redusert samfunnsansvar.
Les også:Penis: mannskapets struktur, hva er varianter og former
Graden av precancerøse endringer i livmorhalsen (CIN)
På bakgrunn av infeksjon med onkogene stammer av humant papillomavirus, skilles tre grader av forstadier til kreft, starter med celleinfeksjon og utseendet på unormale celler som kan utvikle seg til CIN og livmorhalskreft livmor:
1. grad (CINJeg): Lavgradig epitelskade (LSIL). Dette stadiet representerer celleforandringer forårsaket av det humane papillomaviruset, som produserer nye viruspartikler.
2. grad (CINII): høy grad av skade på epitel i livmorhalsen (HSIL). På dette stadiet er precancerøse endringer i cellene mer uttalt. For kvinner som har lignende endringer, er lokal kirurgisk behandling indikert.
Klasse 3 (CINIII): patologisk endrede celler er fordelt gjennom hele tykkelsen på overflatelaget i livmorhalsen og patologiske endringer i cellene øker.
Vedvarende infeksjon med onkogene stammer av humant papillomavirus er en indikator på tilstedeværelsen av forstadier til kreft som CIN I, II og III, og til slutt karsinom in situ (kreft in situ). Invasiv livmorhalskreft følger stadiet av karsinom in situ.
Symptomer
CIN gir ikke et uavhengig klinisk bilde og er asymptomatisk. Smertesyndrom med CIN er som regel alltid fraværende. Kvinnen vet ikke engang at hun har en så farlig sykdom.
Derfor er det viktig å gjennomgå rutinemessige undersøkelser hos din fødselslege-gynekolog hvert sjette måned, siden i i løpet av disse teknikkene, hver gang den viktigste screeningsmetoden for å påvise CIN utføres - en studie av livmorhalsen slag.
Når en sekundær mikrobiell infeksjon er knyttet til CIN, begynner pasienten å klage på leukorré (aka utslipp) fra kjønnsorganet med en uvanlig farge, konsistens eller lukt. Kontaktflekker etter samleie er spesielt bekymringsfullt! Tilstedeværelsen av slike symptomer er en presserende grunn til å konsultere en fødselslege-gynekolog.
Fraværet av spesifikke kliniske symptomer i CIN fremheves i diagnosen ved hjelp av instrumentelle og laboratorieforskningsmetoder.
Diagnostikk
Vår klinikk bruker følgende CIN -diagnostikkprotokoll.
- Gynekologisk undersøkelse ved hjelp av vaginal spekulum - for å oppdage hva som er synlig for øyet endringer i slimhinnen: misfarging, glans rundt det ytre svelget, flekker, spredning av epitelet og dr.
- Cytologisk undersøkelse av et PAP -utstryk fra livmorhalskanalen og den vaginale delen av livmorhalsen kan avsløre atypiske celler og markørceller for papillomavirusinfeksjon. Om nødvendig utfører vi flytende cytologi - den mest moderne og informative diagnostiske metoden.
- Kolposkopi - undersøkelse av livmorhalsen med et kolposkop, en optisk enhet som forstørrer bildet med mer enn 10 en gang og samtidig utføre diagnostiske tester - behandling av livmorhalsen med eddiksyre og en løsning Lugol.
- Om nødvendig utføres en cervikoskopi - undersøkelse av livmorhalskanalen.
- En målrettet biopsi er fjerning av et lite område av livmorhalsvev med identifiserte endringer for histologisk undersøkelse.
- Analyse av cervikal og vaginal avskrapning ved polymerasekjedereaksjon (PCR) for å påvise HPV infeksjoner, etablere typer virus og virusbelastning, som lar deg bestemme taktikken for å behandle pasienten med CIN.
- Ultralydprosedyre.
Behandling
Valget av CIN behandlingsmetode bestemmes av graden av lesjon, størrelsen på lesjonen, kvinnens alder, samtidige sykdommer og pasientens reproduktive planer.
I vår klinikk bruker vi bare moderne metoder for immunstimulerende terapi for HPV -infeksjon og metoder for radiobølgekirurgi, og lager en individuell behandlingsplan for hver kvinne.
Overvåking og forebygging
Det utarbeides en individuell behandlingsplan for hver behandlet pasient. I løpet av det første året utføres 4 kvartalsvise inspeksjoner, hvorunder materialet tas for cytologisk undersøkelse, om nødvendig, PCR -diagnostikk av HPV -infeksjon, kolposkopisk og ultralyd undersøkelser.
Dermed har senteret moderne og effektive metoder for å diagnostisere og behandle CIN i en hvilken som helst grad for å unngå degenerasjon til livmorhalskreft. Tidlig påvisning av sykdommen, passende diagnose og behandling, ytterligere regelmessig medisinsk tilsyn kan kurere nesten alle stadier av sykdommen.
For råd om forebygging, diagnose og behandling av CIN, kontakt fødselslegen-gynekologen ved vårt senter
Kudinov Sergey Viktorovich, kandidat for medisinsk vitenskap.
Du kan også ta en test for cervikal dysplasi (CIN).
Kilde: https://vera-72.com/eto-interesno/tservikalnaya-intraepitelialnaya-neoplaziya-cin.html
Prostatisk intraepitelial neoplasi (PIN) og prostatakreft

Morfologisk prostatakrefti de fleste tilfeller er det representert ved et typisk adenokarsinom.
I følge klassifiseringen av Verdens helseorganisasjon, sammen med godartede papillære adenomer, er det forløpere for kreft, som f.eks. prostata intraepitelial neoplasi (PIN).
Typer kreftskader er representert ved klassisk adenokarsinom og dets forskjellige varianter. I tillegg til det typiske morfologiske bildet av adnokarsinom, har prostatakreft mange varianter av sjeldne typer ondartet neoplasma.
Det er ingen sammenheng mellom en økning i serum PSA (prostata spesifikt antigen) konsentrasjon og tilstedeværelsen og alvorlighetsgraden av IDUer.
PSA -konsentrasjonen hos pasienter med høy og lav grad av IDU skiller seg ikke signifikant fra dataene som er oppnådd hos pasienter med godartede resultater av morfologisk undersøkelse.
Denne økningen bør være forbundet med endringer i prostatavevet som ledsager IDUer: prostatitt hos pasienter med lavgradige IDUer eller kreft som ikke ble oppdaget ved primærbiopsi hos pasienter med høyverdige IDUer.
Fraværet av en direkte påvirkning av IDUer på blod PSA -nivåer bekreftes også ved identifisering av høye og lave IDUer på operasjonsstuen. materiale hos pasienter som ble operert for prostata adenom og ikke hadde mistanke om kreft, inkludert ifølge studien PSA av blod.
Høy kreftdeteksjon ved gjentatte prostatabiopsier selv med normale verdier serum PSA -konsentrasjon lar urologer vurdere IDU som en høy grad av uavhengig risikofaktor for kreft prostata.
Prostatisk intraepitelial neoplasi (PIN) er en forstadier til kreft som er en indikasjon på gjentatt biopsi av prostata. Jo flere kjertler med IDUer blir oppdaget, jo mer sannsynlig er det at prostata adenokarsinom oppdages.
Og dermed, prostata intraepitelial neoplasi (PIN) er den mest sannsynlige prediktoren for prostata adenokarsinom.
For øyeblikket støtter ikke Verdens helseorganisasjon gradering av IDU -er med grader (tidligere ble høye og lave IDU -er skilt). Diagnosen IDU tilsvarer endringer som bare er karakteristiske for høyverdige IDUer. Endringer som er karakteristiske for lavgradige IDUer kalles atypisk hyperplasi.
Behandlingen av pasienter etter oppdagelsen av IDUer i dem er fortsatt stort sett et kontroversielt spørsmål. Det antas at menn med høyverdige IDU-er regelmessig bør screenes med en PSA-konsentrasjon og gjentas biopsier for tidlig påvisning av kreft, siden det er et veldig stort potensial for at de har latent kreft prostata.
I behandling av IDUer identifisere følgende mulige tilnærminger:
- nøye observasjon
- diettterapi
- hormonell og strålebehandling.
Dynamisk kontroll av PSA -nivåer i serum kan betraktes som optimalt.
Høykvalitets prostata intraepitelial neoplasi (PIN) er hormonsensitiv, men effektiv effekten på det er bare mulig med langvarig og aktiv behandling, som kan utføres ved utnevnelse av maksimal androgene blokade.
Les også:
For å kontakte forfatteren av materialet på nettstedet "Prostate", kan du bruke siden "Kontakter"
Kilde: https://prosto-prostata.com.ua/menuprostatitis/mainmenuprostdiagn/55.html
Pagets sykdom; intraepitelial neoplasi; vulvarkreft

Differensialdiagnose av godartede, pre-invasive og neoplastiske sykdommer er en viktig forutsetning for å forbedre behandlingsresultatene.
Pre-invasive sykdommer i vulva
Preinvasive neoplastiske sykdommer i vulva faller i to kategorier: Pagets sykdom og intraepitelial neoplasi av vulva.
Alle områder med kronisk irritasjon av vulva, ledsaget av kløe og resistent mot lokal behandling, spesielt hos postmenopausale kvinner, er underlagt obligatorisk biopsi, eller, i fravær av synlige lesjoner, kolposkopi med målrettet biopsi for å få histologisk diagnose. Histologisk er Pagets sykdom, intraepitelial neoplasi og vulvar melanom ganske like, derfor brukes immunhistokjemisk analyse også for differensialdiagnose.
Pagets sykdom
Pagets sykdom i vulva manifesteres av intraepitelial neoplasi i huden i det anogenitale området.
Omtrent 20% av pasientene med Pagets sykdom har et felles adenokarsinom av en annen lokalisering (bryst, livmorhals, blære, endetarm), som har skjulte trekk.
I disse tilfellene er tumormetastaser vanligvis allerede tilstede. Med unntak av metastatiske lesjoner kan Pagets sykdom behandles lokalt.
Patogenese. Utviklingen av Pagets sykdom er forbundet med kroniske inflammatoriske endringer. Det antas også at Paget -celler kan stamme fra svette og talgkjertler.
Klinikk og diagnostikk. Sykdommen utvikler seg oftere hos kvinner etter 60 år, selv om kløe og vulvodyni naturligvis går foran manifestasjonen av denne sykdommen i årevis.
Et karakteristisk symptom er vedvarende langvarig kløe i vulva, som er forbundet med fløyelsaktig røde flekker på huden, som over tid blir de utsatt for eksematiske endringer og er dekket med hvite plater av hyperkeratinisert epitel og noen ganger - sår.
Pagets sykdom kan påvirke kjønnsleppene, perianalregionen, perineum og har en tendens til å spre seg. Noen ganger er det en samtidig lesjon av brystvorten i brystkjertelen.
Diagnosen bekreftes av vulvarbiopsi og immunhistokjemi.
Behandlingen er ved lokal lokalisering av intraepitelial lesjon (> 5 mm større enn den kanter) med obligatorisk histologisk kontroll av kantene på det fjernede vevet og ekskludering av ledd adenokarsinomer. Men til tross for tilstrekkelig lokal eksisjon kan Pagets sykdom gjentas mange ganger, noe som krever mange gjentatte lokale eksisjoner.
Les også:Hva betyr diagnosen normozoospermi?
Noen ganger er det progresjon til invasiv Pagets sykdom. Minimal dermal invasjon (
Kilde: https://www.eurolab.ua/encyclopedia/patient.gynecology/48697/
Hva jeg hater om atypisk spredning av liten acinar prostata

Tidlig påvisning av prostatakreft har nå blitt hovedoppgaven for urologi. For tiden står alle land overfor problemet med massiv spredning av kreftsykdommer.
I vårt land er prostatakreft den nest vanligste etter hudkreft. Det utgjør en stor fare selv i sammenligning med ondartede svulster i lungene eller magen.
Samtidig øker ikke bare antallet pasienter selv. Dødeligheten av prostatakreft øker også. Urologer forbinder disse dataene med bruk av sykdoms screening og forbedring av prostata biopsiteknologi.
Nå må alle menn etter 45 år gjennomgå denne undersøkelsen.
6-punkts sekstantbiopsimetoden ble utviklet på slutten av forrige århundre. Det innebærer samtidig bruk av transrektal ultralyd. Prostatakreft som følge av biopsi på 12 hovedpunkter sammen med ultralydkontroll oppdages mye oftere.
For en annen biopsi kreves en primær identifisert høy IDU -rate. Steder for atypisk spredning bør også identifiseres. Oftest er prostata adenokarsinom lokalisert i den perifere sonen. Det ser ut som kjertelatypi.
Adenokarsinom ser ut som små kjertler. Cellene deres inneholder små nukleoler. Men samtidig observeres ikke basalceller. Den lobulære strukturen er også fraværende.
Med fokusene på atypiske kjertler i biopsiprøven kan en diagnose av atypisk spredning allerede gjøres. Disse fokusene bør være mistenkelige for videre utvikling av adenokarsinom.
Men samtidig kan ikke disse indikatorene oppfylle kriteriene for prostatakreft. Deres tilstedeværelse er ganske enkelt grunnlaget for en biopsi av prostata en gang til.
I dette tilfellet er atypisk liten acinar -spredning et adenokarsinom. Dette bekreftes av resultatene fra undersøkelsen. Enhver tvil om prostatakreft krever prostatabiopsi. Det utføres ved bruk av den immunhistokjemiske teknikken for farging av vev.
Som et resultat av søknaden deres, kan antallet gjentatte analyser reduseres. De er foreskrevet ved identifisert intraepitelial neoplasi. Disse studiene må utføres med atypisk spredning. Slike tilstander kalles precancerøse tilstander.
De krever ny undersøkelse av prostata.
En korrekt utført prostatabiopsi gir all nødvendig informasjon om mulig forhåndskreft lesjon av prostata. Hun kan også bekrefte tilstedeværelsen av prostatakreft. Denne undersøkelsen lar deg finne plasseringen av svulsten og dens størrelse.
Det gjør det mulig å identifisere perineural invasjon og stadium av tumorcelledifferensiering. Takket være disse indikatorene er det mulig å bestemme sykdomsstadiet og risikonivået etter å ha utført en prostatektomi.
Analyse av resultatene av en prostatabiopsi lar deg velge det beste behandlingsalternativet.
Biopsimateriale tas langs de perifere delene av prostata. Dette gjør det mulig å identifisere prostatakreft på et tidlig stadium. Under den transrektale biopsien skal nålen være vertikal.
Som et resultat er det mulig å skaffe vevsdeler fra hyperplastiske overgangssoner. Analyse av den patomorfologiske biopsien lar deg bestemme alle endringene av ikke-ondartet natur i kjertelepitelet. De bekrefter ofte risikoen for prostatakreft. Disse indikatorene krever også en gjentatt biopsi. Slike tilfeller inkluderer atypi med mistenkt adenokarsinom.
Indikasjonen er også mistanken om spredning. For å diagnostisere en PIN -kode er det nok å finne kjertler med atypiske celler og et intakt basallag i en biopsiprøve. Dette gir grunnlag for separasjon av PIN og adenokarsinom. For tiden regnes en IDU som en forstadier til kreft med varierende grad av neoplasi. Denne indikatoren er uttrykt i graden av manifestasjon av neoplastiske endringer.
I tidlige studier betydde en høy IDU -rate faktisk risikoen for prostatakreft med rebiopsy. Men utvidede biopsier viser en mye lavere prosentandel av denne risikoen.
American Cancer Service anbefaler gjentatt biopsi i noen tilfeller. Dette er nødvendig når det er høye IDU -er. Det vil være viktig å gjøre denne prosedyren etter 3 måneder.
For å forbedre diagnosen, anbefales det å ta prøver fra stedet for atypien.
I fravær av kreft er det viktig å hele tiden overvåke pasienten og måle PSA -nivået. En rektal undersøkelse og ytterligere to gjentatte biopsier bør også utføres. Dette er nok til å oppdage de fleste prostatasvulster. Etter den første forlengede biopsien må den gjentas med metningsteknikken etter 6 eller 12 måneder.
Konseptet med atypisk liten acinar -spredning ble tidligere brukt for å beskrive kjertler med tegn på arkitektonisk og cellulær atypi. De trengte ikke å tilhøre atypisk adenomatøs hyperplasi.
Denne diagnosen gjelder ikke for kreftformer. Han stiller spørsmål ved nederlagets godhet. Derfor er det i dette tilfellet verdt å kontakte en annen spesialist.
For analyse av biopsier kan immunhistokjemiske metoder brukes.
Blant de mest populære markørene er antistoffer mot cytokeratiner. De lar deg identifisere forskjellene mellom ondartede og godartede celler. Dette inkluderer også antistoffer mot p63-proteinet og antistoffer mot alfametylacylkoenzym A-racemase. Når man oppdager prostatakreft, er det viktig å analysere bildet av sykdommen og trekke visse konklusjoner om taktikken for pasientbehandling.
Gleason -klassifiseringssystemet har vært mye brukt for å identifisere stadiet av prostatakreft i mange år. Det gir analyse av vevets histologiske struktur. Men samtidig tar denne teknikken ikke hensyn til de cytologiske tegnene på atypi. En 5-punkts skala brukes til vurderingen. Samtidig betyr 1 punkt en svært differensiert struktur. Liten differensiering er 5 poeng.
Prostatakreft består av flere steder med ulik differensiering. Under studien bestemmes mengden poeng. Det kalles Gleason -summen. Denne indikatoren inkluderer de vanligste punktene i det histologiske bildet av svulsten. Det er nødvendig å bestemme verdien av beløpet og dets komponenter.
Nyere forskning har vist behovet for endringer i Gleason -systemet. Det er ofte ikke sammenfallende med resultatene av prostatektomi og gir ikke en pålitelig vurdering av stadium av tumorutvikling.
På 2000 -tallet ble Gleason -systemet modifisert og introdusert i medisinsk praksis. Det ble supplert med noen endringer. Takket være dette har kvaliteten på diagnostikken blitt betydelig forbedret.
Replikasjon av vurderingsresultater og prosentandelen av samsvar mellom biopsi og RP økte også.
Gleason -systemet spår risiko for tilbakefall etter RP og strålebehandling. Størrelsen på målingene sammenfaller med andre indikatorer. Disse inkluderer serum PSA -nivåer og kreftstadium. Ved å undersøke prostatavevet kan patologen gi en kvalitativ og kvantitativ vurdering av den ondartede lesjonen i prostata.
Studier har vist en positiv sammenheng mellom mengden tumorvev i biopsiprøven og størrelsen. Prosentandelen av tumorvev i biopsiprøven kan bidra til å forutsi dynamikken i PSA -nivåer og sykdomsutfallet.
Foreningen for urologer i Europa har bekreftet like prediktiv verdi av antall svulster i millimeter og i prosent.
Men så langt er det ingen enighet om spørsmålet om den prognostiske verdien av indikatoren for mengden tumorvev som oppnås separat fra andre parametere. For en korrekt prognose må den vurderes sammen med andre faktorer.
Et lite volum av hevelse kan ikke alltid utelukke at biokjemisk og klinisk kreft kommer tilbake etter strålebehandling. Derfor kan den ikke fungere som et kriterium for en positiv prognose.
Perineural invasjon er også viktig for den histomorfologiske vurderingen av biopsien. Det er hovedmekanismen for spredning av kreft. Påvisning av PNI i preparatet regnes av mange forskere for å være et faktum av ekstraprostatisk svulstspredning og biokjemisk tilbakefall etter RP.
Så langt er leger ikke enige om PNI. Rollen som en uavhengig prognostisk faktor etter å ha tatt hensyn til PSA -nivået og Gleason -summen er ikke helt klar. Så langt er forskningsresultatene ganske motstridende.
Dette skyldes det store antallet alternativer eller biopsier som ikke inneholder nerver. De har alltid blitt tolket som negative. Mye forskning må gjøres for å komme til visse konklusjoner.
Korrekt utført prostatabiopsi og profesjonell tolkning av resultatene kan gi riktig prognose ved behandling av prostatakreft. På denne måten identifiseres pasienter som ikke trenger akutt legehjelp.
I henhold til anbefalingene fra US Cancer Service er ventetid aktuelt for pasienter i lav- og middels risikogruppen. Den består i å overvåke pasienten og bare gripe inn når sykdommen utvikler seg.
Den omtrentlige levealderen til disse pasientene bør være minst 10 år.
I tillegg til disse kriteriene vurderer mange forskere andre parametere. Disse inkluderer kinetikken og tettheten til PSA. Andelen positive prøver etter biopsi er også viktig.
Volumet av tumorvev i den verste prøven er også av stor betydning. Problemet med å velge pasienter for observasjon er ganske relevant.
De kan lide mer av feildiagnostisering og behandling.
Kilde: https://kaklechitprostatit.ru/vidy/atipicheskaya-melkoatsinarnaya-proliferatsiya.html